
12. Sınıf Fen Lisesi Kimya Ders Kitabı Cevapları Sayfa 95


“12. Sınıf Kimya Ders Kitabı Cevapları Fen Lisesi Sayfa 95 Meb Yayınları” ulaşabilmek ve dersinizi kolayca yapabilmek için aşağıdaki yayınımızı mutlaka inceleyiniz.
12. Sınıf Fen Lisesi Kimya Ders Kitabı Cevapları Sayfa 95
Lewis yapısı çizilirken şu adımlar takip edilir:
1. Moleküldeki toplam değerlik elektron sayısı hesaplanır.
2. Merkez ve uç atomlar belirlenir.
3. Uygun iskelet yapı belirlenir. Moleküldeki atomlar birbirine tekli kovalent bağ ile bağlanır.
4. İskelet yapıdaki her bir bağ için toplam değerlik elektron sayısından iki elektron çıkarılır.
5. Kalan değerlik elektronları ile önce uç atomların, sonra merkez atomun okteti tamamlanır. Uç atom hidrojense dubleti tamamlanır.
6. Merkez atomun oktetinde eksiklik varsa çoklu kovalent bağ oluşturulur.
Örnek
C2H2 molekülünün Lewis yapısını çiziniz.
Çözüm
Öncelikle hidrojen ve karbon atomlarının elektron dizilişi yazılarak değerlik elektron sayıları bulunur.
1. Toplam değerlik elektron sayısı hesaplanır.
Toplam değerlik elektron sayısı = (2×4)+(2×1) 95 = 10
2. Karbonlar merkez atom, hidrojenler ise uç atomdur.
3. H-C-C-H şeklinde bir iskelet yapı belirlenir ve her bir atom tekli kovalent bağ ile bağlanır.
4. Toplam değerlik elektron sayısından tekli bağdaki elektron sayısı çıkarılır. 10-(3×2)=4 elektron
5. Uç atomlar hidrojen olduğu için oktet tamamlama söz konusu değildir. Bu nedenle kalan 4 elektronla merkez atomların okteti üçlü bağ olacak şekilde tamamlanır.
Alıştırma
Aşağıda verilen moleküllerin Lewis yapılarını çiziniz.
a) O2
b) CH4
c) C2H5OH
ç) HCN
d) HCOOH
- Cevap:
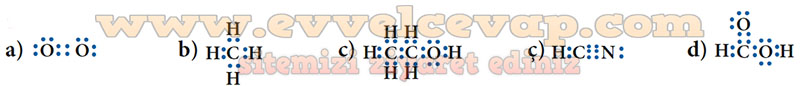
12. Sınıf Fen Lisesi Kimya Ders Kitabı Cevapları Sayfa 95 Meb Yayınları ile ilgili aşağıda bulunan emojileri kullanarak duygularınızı belirtebilir aynı zamanda sosyal medyada paylaşarak bizlere katkıda bulunabilirsiniz.












































